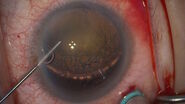
案例描述
一名42岁的白人男性患者被诊断出RPE65基因双等位基因突变,导致莱伯先天性黑蒙。 他患有严重视网膜营养不良症。 他在行政部门工作,养了一只导盲犬,发现在黄昏时走路很困难。
术前评估
患者术前视力很差,患有近视。 进行了全面筛查,显示没有视网膜电图(ERG),包括全灵敏度测试(FST)和多亮度迁移率测试(MLMT)。
术前 OCT 和蓝色自发荧光眼底图像显示光感受器仅出现在中心凹区域和对称的左眼。
手术方法
手术计划如下:进行23g玻璃体切除术,用稀释的曲安奈德对玻璃体进行染色,进行预防性周边激光治疗以避免继发性视网膜脱离,并使用显微注射系统在视网膜下注射300微升基因治疗。
术中 OCT 可检查右眼是否有后玻璃体脱离。 它由脚踏板控制,并具有自动定位功能(图2)。
为了检查是否有后部玻璃体残留,注射了曲安奈德。 然后在黄斑区域进行新的扫描。 自动定位显示一些曲安奈德残留,用 ILM 镊子将其分离。 扫描还显示玻璃体劈裂,这在成年患者中很常见。 如果没有术中 OCT,这一点可能会被错过。
拉动后玻璃体的残余物,用玻璃体切除术探针将其提起,将其分离到玻璃体基底的周边。 在周边激光治疗期间进行玻璃体基底的剃除。
在视网膜下注射之前,外科医生测量视网膜厚度并通过套管针插入视网膜下插管。 术中 OCT 有助于检查插管的位置。 使用显微注射系统进行注射。 一旦水泡被诱导,压力就会降低,使水泡非常缓慢且轻柔地延伸到中央凹。 术中 OCT 的使用支持了整个过程中对滤泡的控制。
将 300 微升基因治疗注射到视网膜下。 术中 OCT 脚踏板允许根据需要移动扫描。
一旦水泡完全形成并注入所有液体,就会进行多次扫描并记录以用于临床试验。 对滤泡表面的扫描可以检查黄斑中心凹的拉伸情况并确认没有黄斑裂孔。 还验证了注射侧,以确保视网膜切除术闭合。
手术结束时,进行了 BSS 液体交换,从而去除任何可能逸入玻璃体的治疗药物,清洁玻璃体并避免炎症反应。 这种机械交换也可能有助于将水泡向后移动一点,以确保所有后段都得到治疗。
术后结果
手术后,由于患者患有严重营养不良,视力仅略有改善。 然而,患者报告说在黄昏时视力更好。 他还表示,他现在能够在晚餐时观察人们的脸,并在晚上区分街上汽车的形状。 此外,他还表示自己不再盯着灯光看。