21 CFR 第 11 部分概述
21 CFR 第 11 部分是由 FDA 引入的,旨在建立电子记录和电子签名的建议。该指南适用于制药和生物技术行业中使用电子文档的所有方面。涵盖的关键领域包括系统验证、审计跟踪、记录保留和用户访问控制。
范围的解释
为了促进创新和技术进步以造福公共健康,并避免不必要的控制和成本,FDA 打算狭义地解释第 11 部分的范围 [1]. 这意味着,对于需要维护或提交给 FDA 的记录,当这些记录以电子格式而非纸质格式使用时,第 11 部分将适用。然而,这一事实不适用于电子记录的纸质打印件,当纸质记录已用于满足所有适用的 FDA 法规和规定的要求时。
第 11 部分记录的定义
第 11 部分适用于以下电子记录 [1]:
- 以电子格式维护的记录,可以替代或补充纸质格式。
- 以电子格式提交给 FDA 的记录。
- 用于执行受监管活动的电子记录,除了纸质文件外。
- 替代手写签名和其他签署方式的电子签名。
注意:建议需要维护的记录的用户提前确定受监管活动将如何执行,即以电子形式还是纸质形式。此决定应明确记录。
细胞培养结果文档的重要性
遵循 21 CFR 第 11 部分的建议对于生物技术和制药行业的细胞培养实验室至关重要,以确保数据完整性、可追溯性和问责制。不遵循这些建议可能会导致重大处罚,包括产品召回、法律后果和市场信任的丧失。
验证
验证计算机系统的决定应考虑用户是否能够满足要求,并确保记录和签名的准确性、真实性和完整性 [1]. FDA 建议该方法应基于文档化的风险评估,以确定系统可能如何影响产品质量、安全性和记录完整性。
实施
为了实施有效的审计追踪:
- 使用自动记录所有用户操作的软件;
- 确保所有修改都有时间戳条目;
- 定期审查和审核记录轨迹,以查找不一致或未经授权的更改。
应遵守所有关于文档的要求,例如日期和时间[1]. 如果没有这样的要求,审计轨迹或其他物理、逻辑或程序安全措施仍然可能对确保记录的可信性和可靠性至关重要。决策应基于定义的要求、风险评估、记录完整性以及产品质量/安全性。
此外,当受监管记录的创建、修改或删除发生时,审计轨迹可能会很有用。
记录的副本
在检查期间,应向调查人员提供适当的记录访问权限 [1]. 电子记录的副本应以常见的电子格式(PDF、XML 或 SGML)提供,使用已建立的软件转换或导出方法。所使用的复制过程应生成保留记录内容和含义的副本。应允许在组织的场所使用其硬件对记录进行可读形式的检查、审查和复制。
记录保留
维护记录的决策应基于定义的要求和记录的风险评估,包括对记录随时间变化的价值的判断 [1]. 重要的是,任何所需记录的副本应保留其内容和含义。记录可以以非电子格式归档,例如微缩胶卷、微缩胶片和纸张,或以标准电子文件格式(例如 PDF、XML 或 SGML)归档。此外,电子和非电子记录及签名可以共存,即混合情况。
Mateo FL 数字式显微镜的优势
为帮助用户遵循 21 CFR 第 11 部分的建议,Mateo FL 显微镜提供以下功能:
- 关于验证、审计追踪和用户管理(上述第 4、5 和 8 节)
- 内置详细的审计追踪和集成的用户管理功能,以便于更轻松和更安全的数据管理;
- 通过条形码扫描功能轻松跟踪和管理样本;
- 关于记录的副本和记录保留(上述第 6 和第 7 节)
- 通过二维码更轻松地将数据共享到任何移动设备;
- 安全的数据跟踪和无缝的数据传输;
- 更实用的文件存储管理 - 可存储高达 300 万张图片,拥有 500GB 的存储空间,从而减少传输或删除文件的时间。
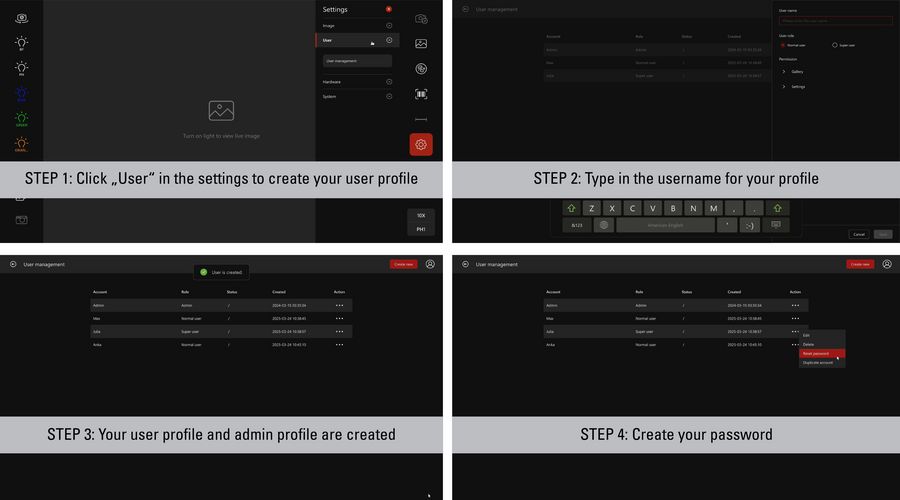
Mateo FL 如何帮助用户满足 21 CFR 第 11 部分关于验证、审计跟踪、记录副本、记录保留和用户管理的建议的示例如下图 2 和图 3 所示。
结论
遵守 21 CFR 第 11 部分对于确保生物技术和制药细胞培养实验室电子记录的完整性和可靠性至关重要。通过专注于强大的审计跟踪和用户管理实践,组织可以满足监管要求并保持最高的数据安全性和可追溯性标准。与基于纸张的记录相比,使用数字式显微镜方法进行细胞培养在电子记录方面的优势在于结果的记录更加一致和高效。
常见问题解答
什么是 21 CFR 第 11 部分,为什么它很重要?
21 CFR 第 11 部分是美国食品药品监督管理局(FDA)针对电子记录和电子签名的指导方针。它帮助用户确保电子记录与纸质记录同样可靠,这对于在生物技术和制药等受监管环境中维护数据完整性和可追溯性至关重要。
Mateo FL 显微镜如何帮助满足 21 CFR 第 11 部分的合规要求?
Mateo FL 提供了合规所需的审计追踪和用户管理功能。它自动记录所有用户操作,并跟踪对记录所做的任何修改,确保数据管理的安全性和可追溯性。
Mateo FL 的哪些功能有助于安全的数据管理?
Mateo FL 允许详细的审计追踪。此外,它通过二维码提供无缝的数据传输,并支持长期数据存储,这对于合规性至关重要。
Mateo FL 显微镜的审计追踪功能可以自定义吗?
Mateo FL 的审计追踪是内置的,捕捉所有相关操作。管理员可以审查审计追踪,以验证操作是否符合监管标准。当启用时,它会记录并保护所有数据,以实现全面可追溯性,支持符合 21 CFR 第 11 部分的要求。
Mateo FL 如何处理数据存储和保留以确保合规?
Mateo FL 提供了 500 GB 的宽裕存储空间,能够存储多达 300 万张图像,确保数据安全保留,无需频繁转移,从而降低合规风险。
不遵循 21 CFR 第 11 部分建议的后果是什么?
不遵循 21 CFR 第 11 部分的建议可能导致不符合 FDA 对生物技术和制药行业的规定,可能会导致重大处罚,包括罚款、产品召回、法律诉讼和市场信任的丧失。实施 Mateo FL 有助于您的实验室满足监管要求。